异氰酸
异氰酸是一种无机化合物,分子式为HNCO,通常写作 H–N=C=O。它是无色的物质,有挥发性,有毒,沸点为 23.5 °C。為氰酸的互變異構體。
| 异氰酸 | |
|---|---|
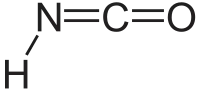 | |
 | |
| IUPAC名 Isocyanic acid | |
| 识别 | |
| CAS号 | 75-13-8 420-05-3(氰酸) ? |
| PubChem | 6347 |
| ChemSpider | 6107 |
| SMILES |
|
| InChI |
|
| InChIKey | OWIKHYCFFJSOEH-UHFFFAOYAE |
| 性质 | |
| 化学式 | HNCO |
| 43.03 g·mol⁻¹ | |
| 外观 | 無色液體或氣體(沸點接近室溫) |
| 密度 | 1.14 g/cm3 (20 °C) |
| 熔点 | -86 °C [1] |
| 沸点 | 23.5 °C |
| 溶解性(水) | 可溶 |
| 溶解性 | 可溶於苯、甲苯、醚 |
| 危险性 | |
| 主要危害 | 有毒 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
异氰酸对应的阴离子 [N=C=O]−
和氰酸一样,也被称作氰酸盐。相关的官能团 –N=C=O 叫做异氰酸酯,是氰酸酯 –O–C≡N、雷酸盐 –O–N+≡C−和氧化腈 –C≡N+–O−的异构体。[2]
异氰酸于 1830年被尤斯图斯·冯·李比希和弗里德里希·维勒发现。[3]
异氰酸是含有碳、氢、氮和氧这四个在有机化学和生物学中最常见的原子组成的稳定分子里,最简单的。它也是四个化学式为 HOCN 的化合物中唯一稳定的,其它三个是氰酸 H–O–C≡N 、雷酸 H–C≡N+–O−[4]和异雷酸 H–O–N+≡C−。[2][5]
性质
制备
异氰酸可以由氰酸盐,例如氰酸钾和气态氯化氢或是像草酸之类的酸反应而成。[14]
- H+ + NCO- → HNCO
HNCO 也可以由三聚体三聚氰酸热分解而成:
- C3H3N3O3 → 3 HNCO
- OC(NH2)2 → HNCO + NH3
其中的异氰酸会迅速聚合成三聚氰酸。
參考资料
- Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- William R. Martin and David W. Ball (2019): "Small organic fulminates as high energy materials. Fulminates of acetylene, ethylene, and allene". Journal of Energetic Materials, volume 31, issue 7, pages 70-79. doi:10.1080/07370652.2018.1531089
- Liebig, J.; Wöhler, F. . Ann. Phys. 1830, 20 (11): 394 [2021-03-28]. Bibcode:1830AnP....96..369L. doi:10.1002/andp.18300961102. (原始内容存档于2018-08-06).
- Kurzer, Frederick. . Journal of Chemical Education. 2000, 77 (7): 851–857. Bibcode:2000JChEd..77..851K. doi:10.1021/ed077p851.
- Donghui Quan, Eric Herbst, Yoshihiro Osamura, and Evelyne Roueff (2010): "Gas-grain modeling of isocyanic acid (HNCO), cyanic acid (HOCN), fulminic acid (HCNO), and isofulminic acid (HONC) in assorted interstellar environments" The Astrophysical Journal, volume 725, issue 2, pages doi:10.1088/0004-637X/725/2/2101
- Nakamoto, part A, p 190
- Teles, Joaquim Henrique; Maier, Günther; Andes Hess, B.; Schaad, Lawrence J.; Winnewisser, Manfred; Winnewisser, Brenda P. . Chemische Berichte. 1989, 122 (4): 753–766. doi:10.1002/cber.19891220425.
- Greenwood, p323
- Wells, p 722
- IUPAC SC-Database (页面存档备份,存于) A comprehensive database of published data on equilibrium constants of metal complexes and ligands
- A. S. Narula, K. Ramachandran “Isocyanic Acid” in Encyclopedia of Reagents for Organic Synthesis, 2001, John Wiley & Sons, New York. doi:10.1002/047084289X.ri072m Article Online Posting Date: April 15, 2001.
- Teles, Joaquim Henrique; Maier, Günther; Andes Hess, B.; Schaad, Lawrence J.; Winnewisser, Manfred; Winnewisser, Brenda P. . Chem. Ber. 1989, 122 (4): 1099–0682. doi:10.1002/cber.19891220425.
- Jacox, M.E.; Milligan, D.E. . Journal of Chemical Physics. 1964, 40 (9): 2457–2460. Bibcode:1964JChPh..40.2457J. doi:10.1063/1.1725546.
- Fischer, G.; Geith, J.; Klapötke, T. M.; Krumm B. (PDF). Z. Naturforsch. 2002, 57b (1): 19–25 [2021-03-29]. S2CID 37461221. doi:10.1515/znb-2002-0103. (原始内容存档 (PDF)于2012-02-05).
- Preidt, Robert. . MyOptumHealth. AccuWeather. [14 September 2011]. (原始内容存档于2011-11-21).
外部链接
- Walter, Wolfgang. . Chichester: Albion Publishing. 1997: 364 [2008-06-21]. ISBN 978-1-898563-37-2. (原始内容存档于2022-04-05).
- Cyanic acid (页面存档备份,存于) from NIST Chemistry WebBook (accessed 2006-09-09)
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.