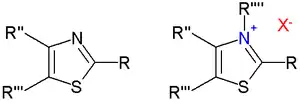
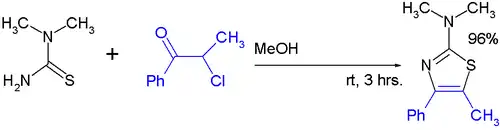
噻唑
噻唑[註 1](英語:),或1,3-噻唑(),是浅黄色可燃液体,气味与嘧啶类似,化学式为C
3H
3NS。它包含一个五元环,其中两个顶点分别是氮原子和硫原子,另外三个是碳原子[1]。
| 噻唑 | |||
|---|---|---|---|
| |||
| 识别 | |||
| CAS号 | 288-47-1 | ||
| PubChem | 9256 | ||
| ChemSpider | 8899 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | FZWLAAWBMGSTSO-UHFFFAOYAI | ||
| ChEBI | 43732 | ||
| 性质 | |||
| 沸点 | 116-118 °C | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
噻唑及其盐
噻唑是一类有这含氮五元环的化合物,均包含一个噻唑官能团。噻唑具有芳香性。
噻唑官能团是维生素B1和埃博霉素的一个至关重要的部分。其他比较重要的噻唑化合物包括苯并噻唑,存在于萤火虫的化学荧光素里。
当噻唑中的氮原子被烷基化后,就形成了一个噻唑盐。在施泰特尔反应和安息香缩合中,噻唑盐可以当作催化剂。噻唑染料也被用来染棉花。
有机反应
噻唑比噁唑拥有一个更大的π电子离域化,所以也更具有芳香性。这个理论被环上氢原子的核磁共振所证明(核磁共振数据介于7.27到8.77之间),体现了一个很强的反磁性环电流。
根据对环上π电子密度的计算,C5是最强的亲电位点,C2是亲核位点。
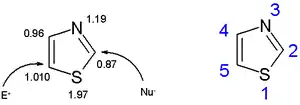
噻唑的电荷密度及环的编号
噻唑的反应性总结如下:
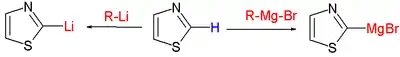
Thiazole deprotonation
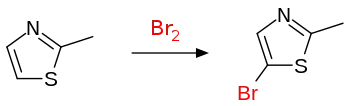
噻唑的溴代
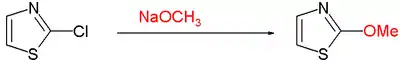
噻唑的亲核取代反应
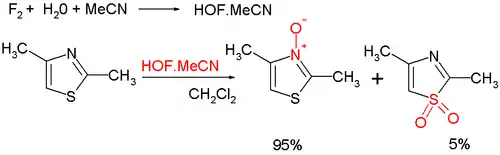
Thiazole oxidation
- 噻唑可以发生环加成反应,但因为本身的芳香稳定性,所以同行需要较高的温度。与炔发生狄尔斯-阿尔德反应伴随着硫的消去,其结果是一个嘧啶。在一项研究中[3] 发现,2-(二甲基氨基)噻唑与乙炔基乙二酸二甲酯发生温和的反应生成嘧啶,发生[2+2]环加成经过了一个两性离子中间体,然后发生4电子电环化开环形成1,3-硫地平,最后最后通过一个电环化关环推出硫原子形成7-thia-2-azanorcaradiene。
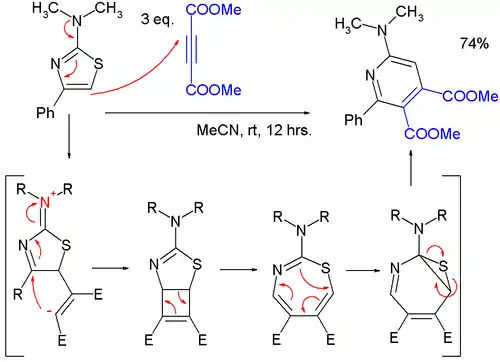
噻唑环加成
参考文献
- The Chemistry of Heterocycles : Structure, Reactions, Syntheses, and Applications Theophil Eicher, Siegfried Hauptmann ISBN 3-527-30720-6
- George Schwarz: 2,4-Dimethylthiazole. 1955.
- Mateo Alajarín, José Cabrera, Aurelia Pastor, Pilar Sánchez-Andrada, and Delia Bautista. . J. Org. Chem. 2006, 71 (14): 5328 – 5339. doi:10.1021/jo060664c.
- Alessandro Dondoni and Pedro Merino: Diastereoselective Homologation of D-(R)-Glyceraldehyde Acetonide using 2-(Trimethylsilyl)thiazole. 1998.
- Elizabeta Amir and Shlomo Rozen. . Chemical Communications. 2006, 2006: 2262 – 2264. doi:10.1039/b602594c.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.