缬氨霉素
缬氨霉素(Valinomycin)是一种抗生素。
| 缬氨霉素 | |
|---|---|
 | |
| 识别 | |
| CAS号 | 2001-95-8 |
| ChemSpider | 21493802 |
| SMILES |
|
| InChI |
|
| InChIKey | FCFNRCROJUBPLU-DNDCDFAIBE |
| ChEBI | 28545 |
| 性质 | |
| 化学式 | C54H90N6O18 |
| 1111.32 g·mol⁻¹ | |
| 外观 | 白色固體 |
| 熔点 | 190 °C(463 K) |
| 溶解性 | 甲醇、乙醇、乙酸乙酯、石油醚、二氯甲烷 |
| λmax | 220 nm |
| 危险性 | |
| 主要危害 | 神经毒性 |
| 致死量或浓度: | |
LD50(中位剂量) |
4 mg/kg(大鼠,口服)[1] |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
缬氨霉素是由數種鏈黴菌屬細胞分離而得,像是S. tsusimaensis和S. fulvissimus。
缬氨霉素會將鉀離子包住,使之疏水性大增,可以穿越細胞膜。[2]缬氨霉素-鉀離子複合物的平衡常數高達106,而相對的其鈉離子複合物的平衡常數僅有10。[3]這種差異造成其特殊的生理意義。
结构
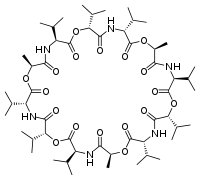
缬氨霉素是一種離子載體,因為他不帶有任何殘基電荷。它由重复三次的D-纈胺酸、L-纈胺酸、D-α-羟基异戊酸盐,和L-乳酸環狀結合,分子間彼此由胺基和酯基結合。結構中的十二個羰基使他可以緊緊抓住中間的金屬離子,且可溶於極性溶劑當中,而當中的異丙基和甲基則使之可溶於非極性溶劑當中[4]。
且對於鉀離子有高度選擇性,不會接受電性及化性相仿的鈉離子[5]。
缬氨霉素的特性來自於他特殊的形狀,他是一個八面體,就像兩個組合起來的金字塔。鉀離子再經過通道時,必須先去水合(也就是離開原先包覆它的水分子)。K+在當中會被纈胺酸的6個羰基牢牢抓住,而鉀離子在當中的空間約為1.33Å,相對的如果包的是鈉離子的話,則空間只有0.95Å,明顯地比離子通道小,代表鈉離子形成離子鍵的能量高過其水合能,無法與胺基酸形成有效的離子鍵結。這導致缬氨霉素對於鉀離子的選擇性比鈉離子大了 10,000 倍。缬氨霉素在極性溶劑中會將羰基暴露在結構表面,而在非極性溶劑則會將羰基包在結構裡面,異丙基露在外面。
外部連結
- Chemical Safety Regulations from New Jersey Department of Health.
- Health information on Scorecard (页面存档备份,存于).
- Valinomycin (页面存档备份,存于) from Fermentek.
- Pesticide Properties DataBase (PPDB) record for Valinomycin
參考文獻
- Gad, S. C.; Reilly, C.; Siino, K.; Gavigan, F. A.; Witz, G. . Drug and Chemical Toxicology. 1985, 8 (6): 451–468. ISSN 0148-0545. PMID 4092618. doi:10.3109/01480548509041069.
- Cammann K. . Top. Curr. Chem. 1985, 128: 219–258.
- Rose, M.C.; Henkens, R.W. . BBA. 1974, 372 (2): 426–435. doi:10.1016/0304-4165(74)90204-9.
- Thompson M and Krull UJ. . Anal. Chim. Acta. 1982, 141: 33–47. doi:10.1016/S0003-2670(01)95308-5.
- Lars Rose, A. T. A. Jenkins. . Bioelectrochemistry (Amsterdam, Netherlands). 2007-5, 70 (2): 387–393 [2019-02-12]. ISSN 1567-5394. PMID 16875886. doi:10.1016/j.bioelechem.2006.05.009. (原始内容存档于2019-10-15).
- Safiulina D, Veksler V, Zharkovsky A and Kaasik A. . J. Cell. Physiol. 2006, 206 (2): 347–353. PMID 16110491. doi:10.1002/jcp.20476.
- (PDF). [2014-11-22]. (原始内容存档 (PDF)于2012-03-15).
- 1.File.tmp/k_potassium.pdf Potassium ionophore Bulletin]
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.