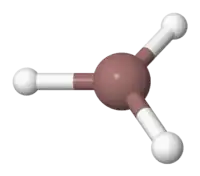
氢化铟
三氢化铟是一种无机化合物,化学式 (InH
3)n。三氢化铟并不溶于所有溶剂。此外,它在标准情况下不稳定。[2]氢化铟在基质分离和激光烧蚀实验中已观察到。[3][4] 气态氢化铟的稳定性也被预测。[5] 它的红外线光谱已由氢气气氛下,气态铟的激光烧蚀获得。[6]三氢化铟是一种硼族元素的氢化物,没有实际用途。
| 氢化铟 | |
|---|---|
 | |
| 系统名 Indigane[1] (substitutive) Trihydridoindium[1] (additive) | |
| 别名 | 三氢化铟 |
| 识别 | |
| CAS号 | |
| PubChem | 24000 |
| ChemSpider | 22435 |
| SMILES |
|
| Gmelin | 163932 |
| ChEBI | 30429 |
| 性质 | |
| 化学式 | InH 3 |
| 117.842 g mol−1 g·mol⁻¹ | |
| 结构 | |
| 配位几何 | 平面三角形 |
| 相关物质 | |
| 相关化合物 | 氢化铝 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
其它铟的氢化物
一些含有 In-H 键的化合物已被报告。[8] 这些例子包含三氢化铟的两个氢原子被其它基团代替而成的 K3[K(Me2SiO)7][HIn(Me3CCH2)3]4[9] 和 HIn(2-Me2NCH2-C6H4)2。
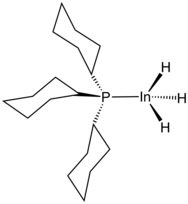
尽管 InH3 本身是不稳定的,它的加合物 InH3Ln (n = 1 或 2)是已知的。[10] 1:1 的胺加合物可以由 LiInH4 和三烷基铵盐反应而成。三甲胺配合物只在 −30 °C 下或稀释溶剂下稳定。 1:1 和 1:2 的三环己基膦(PCy3) 配合物已被发现,其中 In-H 键长平均为 168 pm。[8] 三氢化铟也可以和NHC形成加合物。[11]
参考资料
- . Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute. [2020-03-07]. (原始内容存档于2020-04-11).
- Lester Andrews, Xuefeng Wang. . Angewandte Chemie International Edition. 2004-03-19, 43 (13): 1706–1709 [2020-03-07]. ISSN 1433-7851. doi:10.1002/anie.200353216 (英语).
- Pullumbi, P.; Bouteiller, Y.; Manceron, L.; Mijoule, C. . Chemical Physics. July 1994, 185 (1): 25–37. Bibcode:1994CP....185...25P. doi:10.1016/0301-0104(94)00111-1.
- Aldridge, S.; Downs, A. J. . Chemical Reviews. 2001, 101 (11): 3305–65. PMID 11840988. doi:10.1021/cr960151d.
- Hunt, P.; Schwerdtfeger, P. . Inorganic Chemistry. 1996, 35 (7): 2085–2088. doi:10.1021/ic950411u.
- Andrews, L.; Wang, X. . Angewandte Chemie International Edition. 2004, 43 (13): 1706–1709. PMID 15038043. doi:10.1002/anie.200353216.
- Turley, J. W.; Rinn, H. W. . Inorganic Chemistry. 1969, 8 (1): 18–22. doi:10.1021/ic50071a005.
- Jones, C. . Chemical Communications. 2001, (22): 2293–2298. ISSN 1359-7345. PMID 12240044. doi:10.1039/b107285b.
- Rowen Churchill, M.; Lake, C. H.; Chao, S.-H. L.; Beachley, O. T. . Journal of the Chemical Society, Chemical Communications. 1993, 1993 (20): 1577–1578. doi:10.1039/C39930001577.
- Wang, X.; Andrews, L. . The Journal of Physical Chemistry A. 20 May 2004, 108 (20): 4440–4448. Bibcode:2004JPCA..108.4440W. doi:10.1021/jp037942l.
- Abernethy, C. D.; Cole, M. L.; Jones, C. . Organometallics. 2000, 19 (23): 4852–4857. doi:10.1021/om0004951.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.