四氯化锇
四氯化锇的化学式为OsCl4,是锇的一种氯化物。
| 四氯化锇 | |
|---|---|
 | |
| IUPAC名 Osmium(IV) chloride | |
| 别名 | Osmium tetrachloride |
| 识别 | |
| CAS号 | 10026-01-4 |
| PubChem | 4070891 |
| SMILES |
|
| InChI |
|
| 性质 | |
| 化学式 | OsCl4 |
| 332.041 g/mol g·mol⁻¹ | |
| 外观 | 红色晶体[1] |
| 密度 | 4.38 g/cm3 |
| 沸点 | 450℃(升华) |
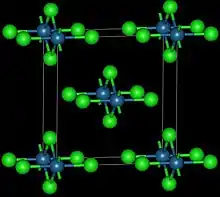
| 结构 | |
| 晶体结构 | Orthorhombic, oS10 |
| 空间群 | Cmmm, No. 65 |
| 相关物质 | |
| 其他阴离子 | 二氧化锇 |
| 其他阳离子 | 氯化铁 三氯化钌 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
四氯化锇可由锇粉在氟硅酸玻璃容器中,和干燥且过量的氧气与氯气在650℃以上反应得到。[1]
- OsO4 + 4 SOCl2 → OsCl4 + 2 Cl2 + 4 SO2
但盐酸作用于四氧化锇只能得到六氯合锇(IV)酸:
- OsO4 + 8 HCl → H2OsCl6 + Cl2 + 4 H2O
性质
四氯化锇在450℃升华,可溶于水并缓慢水解,也可溶于盐酸,但不溶于非极性溶剂。[1]
四氯化锇可以和一些氯化物反应,得到六氯锇(IV)酸盐[1]:
- OsCl4 + 2 MCl → M2OsCl6 (M=碱金属和NH4+)
- 2 OsCl4 —Δ→ 2 OsCl3 + Cl2↑
参考资料
- 《无机化学丛书》.第九卷 锰分族 铁系 铂系. 张青莲 主编. 科学出版社. P347. 3.2 锇的二元化合物
- Paul Machmer. . Chem. Commun. 1967, (12): 610a–610a. doi:10.1039/C1967000610A.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.