肽键
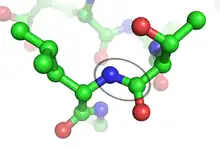
肽鍵

肽鍵形成
生成
兩個胺基酸透過肽鍵生成合為一個二肽,此稱縮合反應。在縮合反應中,兩個胺基酸靠近對方,羧基與氨基相互接近,一個會失去在羧基()上的一氫一氧,另一個則會失去氨基()上的一氫。此反應生成一分子的水() 及被肽鍵()連結的胺基酸,其連結的氨基酸被稱為二肽。
在肽鍵生成時,一胺基酸的羧基會與另一個胺基酸的氨基反應,失去一分子的水(),故過程為脫水反應(也名為脫水縮合)。
形成肽鍵需消耗能量,因而在生物體內,會由ATP提供。[1]肽鍵連結形成的胺基酸鍊會成為多肽與蛋白質。 生物體使用酵素及核糖酶,製造多肽和蛋白質。胜肽由專屬的酶製成,舉例而言,藉由兩種酵素(γ谷氨酰半胱氨酸合成酶、谷氨醯胺合成酶)及兩步驟,可生成三肽的穀胱甘肽。[2][3]
脫水縮合形成酰胺
化學反應

透過水(藍)的親核取代反應,蛋白質會水解(紅)。然而未催化之蛋白質的半衰期可超過幾百年。
由於共振穩定,以生理條件而言是相對穩定,甚至勝過類似的化合物,如酯類。肽鍵在化學反應下可以保持不變,通常會透過陰電性原子攻擊羰基碳,打斷羰基雙鍵形成四面體。這是蛋白水解的過程,而且更常發生在、酰基的交換反應中,好比內含蛋白。
參考文獻
- Watson, James; Hopkins, Nancy; Roberts, Jeffrey; Agetsinger Steitz, Joan; Weiner, Alan. (hardcover) Fourth. Menlo Park, CA: The Benjamin/Cummings Publishing Company, Inc. 1987: 168 [1965]. ISBN 0805396144.
- Wu G, Fang YZ, Yang S, Lupton JR, Turner ND. . The Journal of Nutrition. March 2004, 134 (3): 489–92. PMID 14988435.
- Meister A. . The Journal of Biological Chemistry. November 1988, 263 (33): 17205–8 [2016-10-01]. PMID 3053703. (原始内容存档于2020-06-10).
- Martin RB. (1998) "Free energies and equilibria of peptide bond hydrolysis and formation", Biopolymers, 45, 351–353.
- Goldfarb AR et al. (1951) "The Ultraviolet Absorption Spectra of Proteins", J. Biological Chem., 193, 397–404.(http://www.jbc.org/content/193/1/397.long (页面存档备份,存于))
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.