硼氢化铀
硼氢化铀(IV)是一种无机化合物,化学式为U(BH4)4,是一种绿色易挥发的固体,有放射性。
| 硼氢化铀(IV) | |
|---|---|
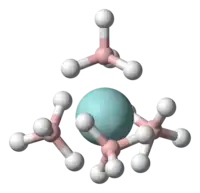 | |
| 别名 | 硼氢化铀 |
| 识别 | |
| CAS号 | 12523-77-2 |
| ChemSpider | 15385433 |
| SMILES |
|
| InChI |
|
| InChIKey | KUMAXXHQRVBPEC-UHFFFAOYAW |
| 性质 | |
| 化学式 | U(BH4)4 |
| 297.4 g·mol⁻¹ | |
| 溶解性(水) | 反应 |
| 溶解性(正庚烷) | 微溶 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
1952年,Hermann I. Schlesinger等人采用铀的四卤化物(UCl4、UF4)和碱金属硼氢化物为原料(如LiBH4)为原料,在无水的液体介质中反应,生成硼氢化铀(IV)[1]:
- UCl4 + 4 LiBH4 → U(BH4)4 + 4 LiCl
Hermann I. Schlesinger等人还用硼氢化铝和铀的四卤化物反应制备U(BH4)4[2]:
- UF4 + 2 Al(BH4)3 → U(BH4)4 + 2 Al(BH4)F2
但硼氢化铝法存在严重的不足,当硼氢化铝遇到微量潮湿的空气时,便会自发性产生猛烈的爆炸。[3]
在Hermann I. Schlesinger之后,В. В. Волков等人用固相的合成方法将四氯化铀在磨球机中粉碎,得到硼氢化铀(IV)[2][4],化学反应方程式如下:
- UCl4 + 4 LiBH4 → U(BH4)4 + 4 LiCl
物理性质
硼氢化铀(IV)为绿色、易挥发的固体(尤其超过30℃时显著挥发[5]),固态时为聚合物。[1]硼氢化铀(IV)微溶于正庚烷和高纯苯。[1]硼氢化铀(IV)有两种晶型。第一种为黄绿色的,第二种为翠绿色的。第二种晶型为正交晶系。溶液中的U(BH4)4会发生离解[1]:
- 3 U(BH4)4 → U(BH4)62- + 2 U(BH4)3+
| 温度/℃ | 蒸汽压/mmHg |
|---|---|
| 34.2 | 0.30 |
| 40.2 | 0.56 |
| 48.25 | 1.23 |
| 54.3 | 2.15 |
| 61.3 | 4.00 |
化学性质
硼氢化铀(IV)和水、醇反应生成氢气。与乙醚反应形成包含硼氢化铀分子的乙醚络合物,该化合物在-80℃比较稳定。[1]硼氢化铀(IV)是活泼的,在空气中缓慢发生反应生成黄色或白色的不挥发性物质。
硼氢化铀(IV)在100℃分解,生成一种不挥发的物质,可自燃,可能是硼氢化铀(III),并在150℃进一步分解,产生UB4和氢气。[5]
应用
硼氢化铀(IV)可以用于铀的同位素的分离。
硼氢化铀在频率I的光的照射下,含235U的化合物会被激发,而含238的不会被激发。同时,用频率II的光照射它们,含有235U的会发生化学分解,而含有238U的不会分解。然后再加热它们,使未分解的升华[6],238U(BF4)4会挥发,而235U(BF4)4在同样的温度下不会挥发。由上述方法可以实现铀的同位素的分离。[1]
硼氢化铀(III)
硼氢化铀(III)是一种无机化合物,化学式为U(BH4)3,在溶液中会发生离解[1]:
- 3 U(BH4)3 → U(BH4)52- + 2 U(BH4)2+
硼氢化铀(III)可以在100℃下热分解硼氢化铀(IV)得到[7]:
- 2 U(BH4)4 → 2 U(BH4)3 + B2H6 + H2
参考资料
- 《硼氢化合物》.郑学家 主编.化学工业出版社. ISBN 978-7-122-11506-5.第五章 其他硼氢化物
- Ephritikhine, M. . Chemical Reviews. 1997, 97 (6): 2193–2242. PMID 11848899. doi:10.1021/cr960366n.
- Ibid., 75, 209(1953)
- В. В. Волков И.Т.Д., Ра∂цохцмця, 18, 512(1976)
- 《无机化学丛书》.张青莲 主编.第一卷.P259.5.2.3 硼氢化铀和硼氢化钍
- 《硼氢化铀的一种简易制备方法》.作者 严家氵甡 严亦君.中国科学院上海有机化学研究所
- 《无机化学丛书》.张青莲 主编.第一卷.P243.5.2 金属硼氢化物MBH4