硅宾
硅宾,又称硅烯、甲硅亚基自由基[1],是一种化合物,化学式为SiH2。它是最简单的卡宾——甲烯——的硅类似物。硅宾在气态下是稳定的,但浓缩时会以双分子方式迅速反应。不像可以以单线态或三重态存在的卡宾,硅宾(及其所有的衍生物)都以单线态存在。
| 硅烯 | |
|---|---|
 | |
 | |
| IUPAC名 Silylene | |
| 系统名 Silylidene | |
| 别名 | Hydrogen silicide(−II) Silicene |
| 识别 | |
| CAS号 | 13825-90-6 |
| PubChem | 6327230 |
| ChemSpider | 4885758 |
| SMILES |
|
| 性质 | |
| 化学式 | H2Si |
| 摩尔质量 | 30.1 g·mol−1 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
硅宾也可以指硅宾的衍生物,其中的氢原子被其它取代基取代。[2]大多数衍生物都含有酰胺基(NR2)或烷基/芳基。[3][4]硅宾被提议为活性中间体。它们是卡宾类似物。[5]
合成和性质
硅宾通常通过聚硅烷的热分解或光解、硅原子的反应(插入或加成)、硅烷的热裂解或1,1-二卤代硅烷的还原合成。长期以来,人们认为金属硅通过硅宾中间体转化为四价硅化合物:
- Si + Cl2 → SiCl2
- SiCl2 + Cl2 → SiCl4
类似的情况适用于Müller-Rochow合成,即氯甲烷和硅的反应。
硅宾的早期观察涉及通过将二甲基二氯硅烷脱氯生成二甲基硅烯:[6]
- SiCl2(CH3)2 + 2 K → Si(CH3)2 + 2 KCl
在三甲基硅烷的存在下进行脱氯,证明了二甲基硅烯的形成,而被捕捉的产物是五甲基乙硅烷:
- Si(CH3)2 + HSi(CH3)3 → (CH3)2Si(H)−Si(CH3)3
一种可以在室温下分离的N-杂环硅宾是N,N′-二叔丁基-1,3-二氮杂-2-环戊硅-4-烯-2-亚基,首次于1994年由Michael K. Denk等人描述。[7]
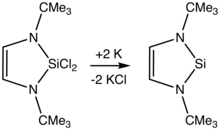
可分离硅宾的合成。
α-酰胺中心通过π供体稳定硅宾。二有机硅二卤化物的脱卤反应受到广泛使用和开发。[8]
有关反应
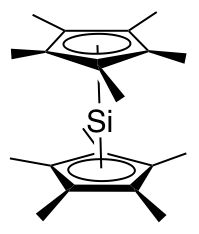
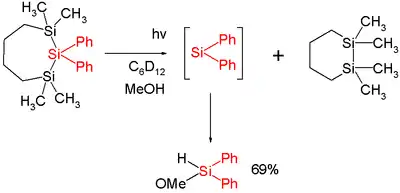
十甲基二茂硅是一种硅宾。[3]
在一项研究中,二苯基硅烯由丙硅烷的闪光光解产生:[9]
在这个反应中,二苯基硅烯从三硅环中挤压出来。这个硅烯可以用520 nm的紫外光谱法观察。它的半衰期很短,只有两微秒。添加甲醇后,它会充当化学捕捉,二级反应速率常数为1.3×1010 mol−1 s−1,接近于扩散控制。
参见
- 卡宾类似物
- N-杂环硅宾
- 硅烯(一类硅氢化合物),R2Si=SiR2
- 硅宾𬭩离子(甲硅亚基正离子),质子化硅宾
参考文献
- 中国化学会有机化合物命名审定委员会. 有机化合物命名原则 2017. 北京:科学出版社, 2018. ISBN 978-7-03-055295-2. p 11-12
- Mizuhata, Yoshiyuki; Sasamori, Takahiro; Tokitoh, Norihiro. . Chemical Reviews. 2009, 109 (8): 3479–3511. PMID 19630390. doi:10.1021/cr900093s.
- Nagendran, Selvarajan; Roesky, Herbert W. . Organometallics. 2008, 27 (4): 457–492. doi:10.1021/om7007869.
- Haaf, Michael; Schmedake, Thomas A.; West, Robert. . Accounts of Chemical Research. 2000, 33 (10): 704–714. PMID 11041835. doi:10.1021/ar950192g.
- Gaspar, Peter; West, R. . Chemistry of Organic Silicon Compounds. The Chemistry of Functional Groups 2. 1998: 2463–2568. ISBN 0471967572. doi:10.1002/0470857250.ch43.
- Skell, P. S.; Goldstein, E. J. . Journal of the American Chemical Society. 1964, 86 (7): 1442–1443. doi:10.1021/ja01061a040.
- Denk, Michael; Lennon, Robert; Hayashi, Randy; West, Robert; Belyakov, Alexander V.; Verne, Hans P.; Haaland, Arne; Wagner, Matthias; Metzler, Nils. . Journal of the American Chemical Society. 1994, 116 (6): 2691–2692. doi:10.1021/ja00085a088.
- Driess, Matthias; Yao, Shenglai; Brym, Markus; Van Wüllen, Christoph; Lentz, Dieter. . Journal of the American Chemical Society. 2006, 128 (30): 9628–9629. PMID 16866506. doi:10.1021/ja062928i.
- Moiseev, Andrey G.; Leigh, William J. . Journal of the American Chemical Society. 2006, 128 (45): 14442–14443. PMID 17090011. doi:10.1021/ja0653223.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.