四氧化二锑
四氧化二锑是一种无机化合物,化学式为Sb2O4。这种物质存在于黄锑矿(cervantite)中。[2]它是白色固体但在加热时可逆的变黄。这种物质的最简式为SbO2,但被称作四氧化二锑来表明其中有两种价态的锑原子。
| 四氧化二锑 | |
|---|---|
 | |
| IUPAC名 氧化锑(III,V) | |
| 识别 | |
| CAS号 | 12786-74-2(SbO2) 1332-81-6(Sb2O4) |
| PubChem | 74002 |
| 性质 | |
| 化学式 | Sb2O4 |
| 307.5176 g·mol⁻¹ | |
| 外观 | 白色固体 |
| 密度 | 6.64 g/cm3(正交晶系) [1] |
| 熔点 | 分解 |
| 沸点 | 分解 |
| 溶解性(水) | 不溶 |
| 折光度n D |
2.0 |
| 结构 | |
| 晶体结构 | 正交晶系 |
| 危险性 | |
| NFPA 704 |
 1
2
0
|
| 相关物质 | |
| 相关化学品 | 三氧化二锑 五氧化二锑 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备与结构
- Sb2O3 + 0.5 O2 → Sb2O4 ΔH = −187 kJ/mol
800°C时,五氧化二锑分解也可制备它:
- Sb2O5 → Sb2O4 + 0.5 O2 ΔH = −64 kJ/mol
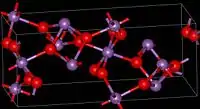
其中锑有两种氧化态,分别是+3和+5。目前已发现两种晶型,一种是正交晶系(右侧图片),另一种是单斜晶系。[1]两种晶型都是六配位的锑(V)中心原子在原位,而变形的锑(III)原子与四个氧原子成键。
参考资料
- J. Amador, E. Gutierrez Puebla, M. A. Monge, I. Rasines, and C. Ruiz Valero "Diantimony Tetraoxides Revisited" Inorganic Chemistry 1988, Volume 27, pp. 1367–1370. doi:10.1021/ic00281a011
- . Webminerals. [2009-06-06]. (原始内容存档于2009-07-14).
- Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.