克莱森重排反应
克莱森重排反应,又稱作Claisen重排反应,其最初形式是一个烯丙基苯基醚在高温(> 200°C)下发生的一个重排反应,产物是邻位烯丙基苯酚。反应的机理是σ[3,3]重排(是史上第一个发现的σ[3,3]重排反应),产物4-烯酮因芳香性的需要互变异构为酚。
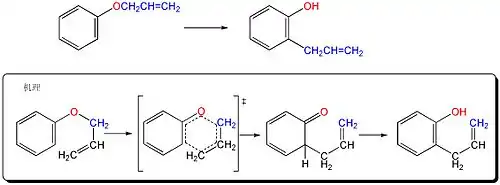
克莱森重排反应
这个反应的特点是高度的区域选择性,产物大部分是邻位的。与弗赖斯重排的性质很相似。
而当苯环的两个邻位都被“堵”住的时候,反应产物是对位烯丙基取代物。这是因为中间产物发生了一个科普重排反应所致——“分子自有其道(molecules have a way of hanging on)”。
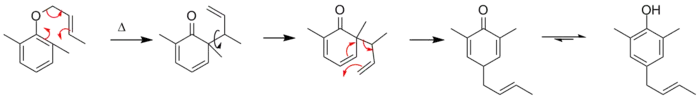
审视整个过程可以看到:克莱森重排的驱动力是生成热力学上最稳定的取代度最大的“烯烃”。
克莱森重排起初是在芳香化合物中发现的(1912年),这与当时(20世纪初期)合成化学家“玩”的范围局限在芳香烃上有关。到后来发现该反应可以拓展到非芳香化合物,而这种拓展非常重要,因为克莱森重排反应立刻变成了合成上一个非常有用的反应:反应生成了一个新的碳碳键,得到一个4-烯羰基化合物,而烯键可以继续往下做衍生,得到其他的化合物。

而现代有机合成在克莱森反应的启发下催生出众多“变体”:
贝勒斯(Bellus)变体:
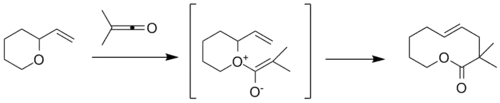
埃申莫瑟(Eschenmoser)变体:
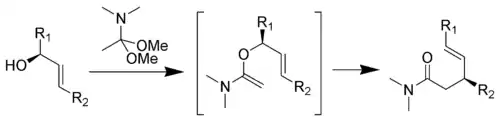
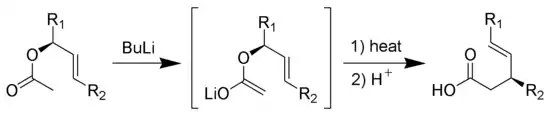
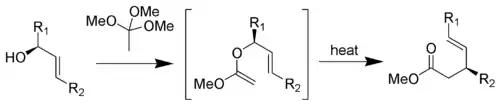
强生(Johnson)变体:
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
