乙矽烷
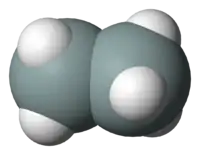
乙矽烷(英語:),又稱矽乙烷,是一種有毒的化合物,分子式為Si2H6,在室溫下为气態。它的性質與乙烷很類似,都是無色易燃的氣體,但是它的矽-矽鍵比乙烷的碳-碳鍵還來的弱,因此比乙烷還不穩定。乙矽烷通常是氫很好的來源,只要經過簡單的化學反應就可以得到氫。另外它也可以用來以薄膜沉積製備純矽,是半導體工業重要的特用電子級氣體之一[3]。
| 乙矽烷 | |
|---|---|
 | |
 | |
| 识别 | |
| CAS号 | 1590-87-0 |
| PubChem | 74123 |
| ChemSpider | 66736 |
| SMILES |
|
| InChI |
|
| InChIKey | PZPGRFITIJYNEJ-UHFFFAOYAQ |
| Gmelin | 368 |
| ChEBI | 30597 |
| 性质 | |
| 化学式 | Si2H6 |
| 62.219 g·mol⁻¹ | |
| 外观 | 無色可燃氣體 |
| 密度 | 2.66 kg/m3(15℃)[1] 0.69 g·cm−3(−25 °C)[1] |
| 熔点 | -132.5 °C(141 K)([1]) |
| 沸点 | -14.5 °C(259 K)([1]) |
| 溶解性(水) | 分解[1] |
| 蒸氣壓 | 2940.2±0.0 mmHg at 25°C[2] |
| 结构 | |
| 分子构型 | 三斜晶系 |
| 偶极矩 | 0 |
| 危险性 | |
| 主要危害 | 可燃,對皮膚會造成刺激 |
| 闪点 | 非常容易閃燃 |
| 相关物质 | |
| 相关矽烷 | SiH4 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
乙硅烷通常由硅化镁的水解而成。反应会产生甲硅烷、乙硅烷、甚至丙硅烷。该方法已被放弃用于生产甲硅烷,但它仍然可以用于生产乙硅烷。[4]痕量乙硅烷的存在是该方法产生的甲硅烷自燃的原因(类似地,二磷烷通常是磷化氢样品中自发自燃的污染物)。
应用
甲硅烷和乙硅烷在 640 °C下分解,会沉积非晶硅。这个化学气相沉积过程与光伏器件的制造有关。[4]它用于生产硅晶圆。[7]
乙硅烷气体可用于控制 SiC 热分解生长石墨烯过程中,Si 蒸气的压力。 Si蒸气的压力会影响生产的石墨烯的质量。[8]
参考资料
- Record of Disilan in the GESTIS Substance Database from the IFA
- . [2021-07-11]. (原始内容存档于2021-08-09).
- (PDF). [2018-07-02]. (原始内容 (PDF)存档于2015-09-21).
- Barry Arkles "Silicon Compounds, Silanes" in Kirk-Othmer Encyclopedia of Chemical Technology John Wiley & Sons, New York, 1997. DOI: doi:10.1002/0471238961.1909120101181112.a01.
- US Patent 4,604,274
- P. W. Schenk "Silanes" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 680.
- Disilane 的存檔,存档日期September 27, 2004,.
- Mishra, N. , Boeckl, J. , Motta, N. and Iacopi, F. (2016), Graphene growth on silicon carbide: A review. Phys. Status Solidi A, 213: 2277-2289. doi:10.1002/pssa.201600091 (check page 2280)
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.