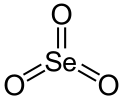
三氧化硒
三氧化硒(化学式 SeO3)是硒(VI)的氧化物,为白色潮解性晶体。它也是一种氧化剂和路易斯酸,可以制备其它Se(VI)化合物。[3]
| 三氧化硒[1] | |||
|---|---|---|---|
| |||
| 识别 | |||
| CAS号 | 13768-86-0 | ||
| PubChem | 115128 | ||
| ChemSpider | 103019 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | VFLXBUJKRRJAKY-UHFFFAOYAC | ||
| 性质 | |||
| 化学式 | SeO3 | ||
| 126.96 g·mol⁻¹ | |||
| 外观 | 白色潮解性晶体 | ||
| 密度 | 3.44 g/cm3 | ||
| 熔点 | 118.35 °C | ||
| 沸点 | 升华 | ||
| 溶解性(水) | 溶解度很大 | ||
| 结构 | |||
| 晶体结构 | 四方晶系 | ||
| 危险性 | |||
| 欧盟分类 | |||
| NFPA 704 |
 0
4
2
OX
| ||
| 致死量或浓度: | |||
LD50(中位剂量) |
7 mg/kg(大鼠,口服) 7.08 mg/kg(小鼠,口服) 5.06 mg/kg(豚鼠,口服) 2.25 mg/kg(兔子,口服) 13 mg/kg(马,口服)[2] | ||
LC50(中位浓度) |
13 mg/kg(猪,口服) 9.9 mg/kg(牛,口服) 3.3 mg/kg(山羊,口服) 3.3 mg/kg (绵羊,口服)[2] | ||
| 相关物质 | |||
| 其他阴离子 | 六硫化二硒 | ||
| 其他阳离子 | 三氧化硫 三氧化碲 三氧化钋 | ||
| 相关化学品 | 二氧化硒 硒酸 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
制备
三氧化硒难以制备,因为它对分解成二氧化硒的反应并不稳定:
- 2 SeO3 → 2 SeO2 + O2
实验室通过用无水硒酸钾(K2SeO4)和三氧化硫反应制备三氧化硒:[4]
- K2SeO4 + SO3 → SeO3 + K2SO4
反应
SeO3 的化学性质比起三氧化碲 TeO3,更像三氧化硫 SO3。[3]
在120 °C下,SeO3和二氧化硒反应,形成混合价态化合物五氧化二硒:[5]
- SeO3 + SeO2 → Se2O5
- 2SeO3 + SeF4 → 2SeO2F2 + SeO2
类似SO3,它也能和如吡啶、二氧六环和乙醚的路易斯碱形成加合物。[3]
它和氧化锂和氧化钠反应,形成 SeVIO54− 和SeVIO66−的盐:[6]它和Li2O的反应会产生Li4SeO5,含有三角双锥结构的 SeVIO54− 阴离子。水平方向的Se-O键长为170.6–171.9 pm,而垂直方向的 Se−O 键较长,为 179.5 pm。它和Na2O的反应产生的是 Na4SeO5,其中的 SeVIO54−离子为四方锥结构。它的Se−O 键长在172.9 至181.5 pm的范围内,而Na12(SeO4)3(SeO6)则含有八面体形结构的 SeVIO66−。SeVIO66− 是未知的原硒酸 (Se(OH)6)的共轭碱。
结构
固态的三氧化硒是由环状的四聚体Se4O12组成的,其中含有(Se-O)4八元环。硒原子是四配位的,桥接 Se−O 键长为 175 pm 和181 pm,而非桥接Se-O键长则为 156 和154 pm。[6]
气态中的SeO3则是四聚体和平面三角形构型的 SeO3 单体的混合物,它的 Se−O 键长为 168.78 pm。[7]
参考资料
- Lide, David R. 87. Boca Raton, Florida: CRC Press. 1998: 4–81. ISBN 0-8493-0594-2.
- . Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry, Elsevier ISBN 0123526515
- Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 422.
- Z. Žák "Crystal structure of diselenium pentoxide Se2O5" Zeitschrift für anorganische und allgemeine Chemie 1980, volume 460, pp. 81–85. doi:10.1002/zaac.19804600108
- Handbook of Chalcogen Chemistry: New Perspectives in Sulfur, Selenium and Tellurium, Franceso A. Devillanova, Royal Society of Chemistry, 2007, ISBN 9780854043668
- Brassington, N. J.; Edwards, H. G. M.; Long, D. A.; Skinner, M. . Journal of Raman Spectroscopy. 1978, 7 (3): 158–160. ISSN 0377-0486. doi:10.1002/jrs.1250070310.
- Max Schmidt, Irmgard Wilhelm: Lösungen von Selentrioxid. In: Chemische Berichte. 97, 1964, S. 872–875, doi:10.1002/cber.19640970334.
- Jane E. Macintyre. . CRC Press. 1992-07: 3128. ISBN 0412301202.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.